
|
| |||
|
Разделы
Главная
Сапромат
Моделирование
Взаимодействие
Методы
Инновации
Индукция
Исследования
Факторизация
Частоты
Популярное
Как составляется проект слаботочных сетей?
Как защитить объект?
Слаботочные системы в проекте «Умный дом»
Какой дом надежнее: каркасный или брусовой?
Как правильно создавать слаботочные системы?
Что такое энергоэффективные дома?
|
Главная » Водородная связь Водородная связь в структуре твердых растворов KxNH4(i-x)C1O4. Халиуллин Р. Ш. (rafik@kemsu.ru), Леонтьева Е. В., Невоструев В. А. Кемеровский государственный университет В последнее время много внимания уделяется изучению различных неорганических сокристаллизованных систем на основе солей аммония [1,2]. Интерес к ним вызван перспективностью этих систем для современного материаловедения в различных областях. Часто наблюдаются не совсем обычные свойства, имеющие порой критическую зависимость от состава. На наш взгляд, при объяснении многих наблюдаемых свойств подобных аммоний содержащих систем незаслуженно забывается способность ионов аммония к образованию водородных связей. Для определения вклада способности ионов аммония к образованию водородных связей нами была изучена система перхлорат аммония - перхлорат калия. Перхлорат аммония - известное соединение, имеющее трехмерную сетку водородных связей. Таким образом, представляло интерес изучить структурно чувствительные свойства в твердых растворах по мере изменения структуры и числа водородных связей при введении ионов калия, не способных к образованию водородных связей. При анализе полученных результатов учитывались материалы обзора [3], указывающего на возможность образования водородных связей между различными элементами с учетом угловых критериев. В данной статье представлены результаты изучения смешанных кристаллических образцов KxNH4(1.x)ClO4 методами химического и рентгенофазового анализа и ИК-спектроскопии диффузного отражения. Образцы получали сокристаллизацией из водных растворов. Определение количественного состава образцов проводили спектрофотометрическим (ионы аммония) и пламенно- фотометрическим (ионы калия) методами. Структуру образцов исследовали методами рентгенофазового анализа и ИК - спектроскопии диффузного отражения. Расчет параметров элементарной ячейки проводили исходя из пространственной группы Pnma методом МНК с использованием квадратичных форм ромбической сингонии. Колебательные спектры регистрировали с использованием программного пакета IR Data Manager при комнатной температуре на ИК Фурье-спектрометре System 2000 FT-IR фирмы Perkin-Elmer в диапазоне часто 450-5000см-1 с разрешением 2см-1. Для анализа спектров использовали программу Grath builder . Первичную информацию о структурообразовании в системе KClO4-NH4ClO4 можно извлечь из данных по сокристаллизации компонентов. На рис.1 приведена кривая распределения аммония между твердой фазой и раствором. Характерной особенностью полученной зависимости является наличие двух линейных участков с существенно отличающимися углами наклона и нелинейной переходной области (~50мол.% аммония в твердой фазе). Безусловно, одной из причин такого неравномерного распределения является существенная разница величин растворимости компонентов. Растворимость перхлората аммония в несколько раз превышает растворимость перхлората калия. Вследствие этого, несмотря на высокую концентрацию NH4ClO4 в растворе (до 75 мол. % относительно исходного соотношения твердых компонентов), эффективность перехода его в кристалл чрезвычайно мала. Коэффициент распределения составляет ~0,1. Дальнейшее увеличение содержания аммония в растворе приводит к значительному повышению константы распределения, значение которой составляет ~0,3-0,9. С(МТ+) ф ,мол.% v 4 тв.фаза 100 80 60 40 20 С(1\1Н+) ф ,мол.% v 4 тв.фаза С(1\Н4 )р-р , мол.% Рис. 1 Кривая распределения перхлората аммония между жидкой и твердой фазами в системе KCIO4 -NH4CIO4 Методом рентгенофазового анализа рассчитаны параметры элементарной ячейки смешанных кристаллов. Зависимости их от состава, как видно на рис.2, неаддитивны. Объем элементарной ячейки кристаллов в области концентраций 0-50 мол. % NH4ClO4 характеризуется отрицательным отклонением от аддитивности и практически совпадает с характерными значениями для индивидуального перхлората калия. В области концентраций 50-100 мол.% NH4ClO4 изменение объема ячейки подчиняется правилу Вегарда. V, 0A 80 100 NH4QO4 , мол.% Рис. 2. Зависимость объема элементарной ячейки от состава твердого раствора KXNH4(1-X)ClO4. Наблюдаемый характер зависимости объема ячейки от состава твердого раствора KXNH4(1-X)ClO4 можно объяснить двумя особенностями природы катиона аммония. Во-первых, катион NHi+представляет собой многоатомный ион с несферической пространственной формой (в отличие от катионов калия), поэтому обладает способностью встраиваться в решетку, незначительно искажая её. В результате - незначительное увеличение параметров ячейки в области 0-50 мол. % NH4ClO4. Во-вторых, наличие протонов в составе катиона аммония определяет образование трехмерной сетки водородных связей с атомами кислорода в структуре NH4ClO4. При изоморфном замещении катионов аммония на катионы калия, меньшие по размеру, но не способные к образованию водородных связей, происходит нарушение пространственной структуры Н-связей и уменьшение объема кристаллической решетки. Разная природа связей в твердых растворах разного состава определяет особенности распределения компонентов между фазами при сокристаллизации и закономерно приводит к разрыву смесимости в области ~50 мол. % компонентов. Для проверки предлагаемой гипотезы о структуре твердых растворов KXNH4(1-X)ClO4 мы исследовали образцы методом колебательной спектроскопии, поскольку предполагаемые см 942940938936- 464 460 456 452 -1 650 640 630 620 cnh4 мол-% см 942 20 40 60 80 100 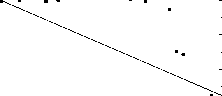 см 464 0 20406080100 cnh4 мол.% 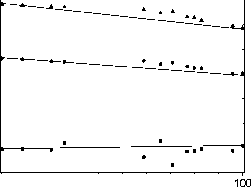 -1 см 650 640 630 620 0 2040 6080 Рис.3. Изменение частот внутримолекулярных колебаний ClO4-с составом твердого раствора KXNH4(1-X)ClO4: а - v1(A1), , б - у2(Е), в - у4(Т2) а б в изменения в структуре двойной системы должны отразиться и на внутримолекулярных колебаниях связей как перхлорат-аниона, так и катиона аммония. Установлено, что в ИК спектрах смешанных кристаллов KXNH4(1-X)ClO4, также как и индивидуальных перхлоратов калия и аммония, наблюдаются четыре основных полосы поглощения перхлорат-аниона: у1(А1), - ассиметричное валентное колебание;у2(Е) -деформационное колебание; у3(Т2)- симметричное валентное колебание и у4(Т2)-деформационное колебание. Отнесение полос проведено согласно [4,5]. Число активных полос поглощения и расщепление полос вырожденных колебаний указывают на понижение симметрии перхлорат-аниона, по крайней мере, до C2V, что характерно и для чистых перхлоратов калия и аммония [g]. Анализ зависимостей частот колебаний v1(A1), у2(Е), v4(T2) ClO4- от состава (рис.3 а-в) показывает их явную неаддитивность. Характер изменения частот колебаний коррелирует с изменением объема элементарной ячейки твердого раствора KXNH4(1-X)ClO4 при увеличении концентрации аммония в образцах. Колебанию v3(T2) в ИК-спектрах перхлоратов соответствует одна широкая полоса с неразрешенной структурой, обусловленной расщеплением вырожденных колебательных уровней. Перекрывание полос компонент колебания v3(T2) затрудняет точное определение значений частот колебаний. Помимо колебаний связей Cl-O в ИК-спектрах смешанных кристаллов наблюдаются полосы, соответствующие колебаниям связей N-H, интенсивность которых увеличивается с ростом содержания аммония в образцах (рис.4,5). 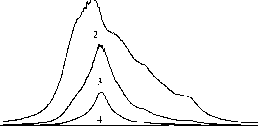 3600 3200 2800 2400 Рис.4. ИК-спектры кристаллов KXNH4(1-X)ClO4 в области валентных колебаний N-H связи: 1- М14СЮ4 , 2 - K0,4NH4(0,6)ClO4 , 3 - K0,8NH4(0,2)ClO4 , 4 - KClO4. 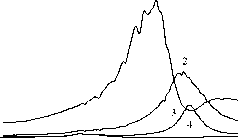 1 7 0~V 1 6 0 0 1 5 0 0 140 0 Рис.5. ИК-спектры кристаллов KXNH4(1-X)ClO4 в области деформационных колебаний N-H связи: 1- М14СЮ4 , 2 - K0,4NH4 (0,6)ClO4 , 3 - K0,8NH4(0,2)ClO4 , 4 - КСЮ4. Доминирующее значение в спектроскопии водородной связи и оценке ее прочности имеют полосы характеристических Н-колебаний, в данном случае N-H связи. Как видно на рис.6, зависимость частоты валентного колебания связи N-H от содержания аммония в твердом растворе носит нелинейный характер. -1 -1 3340- - 3340 332Ы п3320 3300- j 3300 0 20 40 60 80 100 CNH4, мол.% Рис.6 Изменение частоты валентного колебания N-H с составом твердого раствора KXNH4(1-X)ClO4. Характер зависимости согласуется с изменением параметров решетки и частот колебаний перхлорат-аниона. А именно, в области 0-50 мол. % аммония исследуемые параметры не меняются, а в области 50-100 мол. % объем ячейки и частота валентных колебаний N-H увеличиваются, частоты колебаний Cl-O - уменьшаются с увеличением концентрации аммония в образцах. Учет образования водородных связей между катионом аммония и перхлорат-анионом может объяснить экспериментальные результаты. 1. Область концентрации 50-100 мол. % аммония. - Замещение аммония на калий приводит к нарушению трехмерного пространственного остова из Н-связей кристаллической решетки перхлората аммония и образованию ограниченных по протяженности цепей. С увеличением концентрации калия протяженность цепей водородных связей уменьшается и для твердого раствора состава 1:1 при статистическом распределении катионов по узлам решетки Н-связи становятся одиночными. - Можно рассматривать не протяженность и пространственную структуру Н-связей, а их количество. Соответственно, с уменьшением содержания аммония в твердом растворе количество водородных связей уменьшается. В колебательных спектрах эти изменения сопровождаются изменением частот характеристических колебаний. 2. Область концентраций 0-50 мол. % аммония. Перегиб зависимостей исследуемых параметров, вероятно, отражает радикальное изменение структуры твердого раствора. Тогда неизменность частот характеристических колебаний Cl-O и N-H в твердых растворах в данном диапазоне концентраций может быть следствием полного отсутствия взаимодействия между ионами, либо между протонами катиона аммония и атомами кислорода перхлорат-аниона, но образованием Н-связи с атомом хлора. В обоих случаях катион аммония входит в кристаллическую решетку перхлората калия иным образом, чем в перхлорате аммония, а именно тетраэдр NH44 располагается ориентированно в катионном узле. Причем направленность связей N-H по отношению к Cl-O такова, что связь N-H--- O не образуется. Такой способ вхождения катиона аммония в решетку KClO4 объясняет неизменность параметров элементарной ячейки. Экспериментально полученные зависимости изменения частот v2 и v4 колебаний N-H с составом образцов полностью коррелируют с изменением энергии валентных колебаний и подтверждают высказанные предположения о структуре твердого раствора KXNH4(1-X)ClO4 . Таким образом, свойства и структура твердых растворов KXNH4(1-X)ClO4 с содержанием аммония 0-50 и 50-100мол.% существенно различаются. В первой области наблюдается ориентированное вхождение катиона аммония в структуру, причем связь типа N-H--- O не образуется, что определяет неизменность параметров элементарной ячейки и частот характеристических колебаний молекулярных ионов. Во второй области структура Литература 1. P.K. Kaho, X. Lao, M.B. Costello, N.S. Dalal J.Phys.: Condens. Matter., 1994, V.6, P.2971-2974. 2. S. Karan, S. Sen Gupta, S.P. Sen Gupta Material Letters, 2003, V.57, p.4328-4331.. 3. Зефиров Ю.В. Кристаллохимия. 1999. T.44. N.6. С.1091-1093. 4. H.D.Lutz, R.A.Becker, H.J.Berthold, W.Eckers, B.G.Holsher. Spectrochimica Acta, vol.39A, №1, pp.7-14, 1983. 5. M.A.Lopez-Bote, S.Montezo. Journal of Raman spectroscopy, vol.9, №6, 1980. 6. S.K.Syal, S.R.Yoganarasimnan. Journal of Solid State Chemistry1974 ,10, 332-340. перхлората аммония и твердых растворов на его основе характеризуется образованием водородных связей между протонами катиона аммония и атомами кислорода перхлорат-аниона. Катионы калия нарушают систему трехмерных сетей N-Н-O связей, что определяет изменение частот колебаний и параметров элементарной ячейки. Обнаруженные особенности состояния системы KXNH4(1-X)ClO4 практически полностью коррелируют с особенностями поведения данной системы при фотохимическом и радиационно-стимулированном разложении. |
|
| |||